「病原菌検出アッセイ」が輸出検査の正式手法として通知に掲載
2025年5月28日、農林水産省より発出された通知
「アメリカ合衆国向け輸出食肉認定施設における牛肉からの腸管出血性大腸菌(STEC)の検査法について」において、
ネオジェンジャパンの「病原菌検出アッセイ2 STEC 遺伝子スクリーニング(stx/eae)用(MDA2STXEAE48)」が、スクリーニング検査法の一例として正式に認められました。
従来はO抗原の血清型による特定が重視されてきましたが、近年では日本や米国をはじめとする諸外国において、病原性関連遺伝子の検出をスクリーニングの入口とし、その後に血清型の確認を行う多段階の検査法が普及してきています。
今回の通知改正は、こうした国際的な検査の考え方を反映したものであり、日本においても検査法の転換点となる重要な動きといえます。

なぜ今、STEC検査の考え方が変わったのか?
これまで、STEC(腸管出血性大腸菌)の検査は、国内で重症化の報告が多かった6つの血清型(O抗原)― O26、O45、O103、O111、O121、O145 ―を中心に行われてきました。
ところが最近では、この6つに該当しないO抗原を持つ菌による食中毒事例が国内外で増えてきています。 詳細はこちら
こうした状況を受け、欧米では「O抗原の種類にとらわれず、菌が病原性を持っているかという本質で見極める」方法へと移行してきています。具体的には、ベロ毒素を作る遺伝子(stx)と、腸管に付着するための遺伝子(eae)を同時に保有しているかどうかを検出するスクリーニング法です。この2つの遺伝子の組み合わせこそが、人に対して病原性を発現する鍵となります
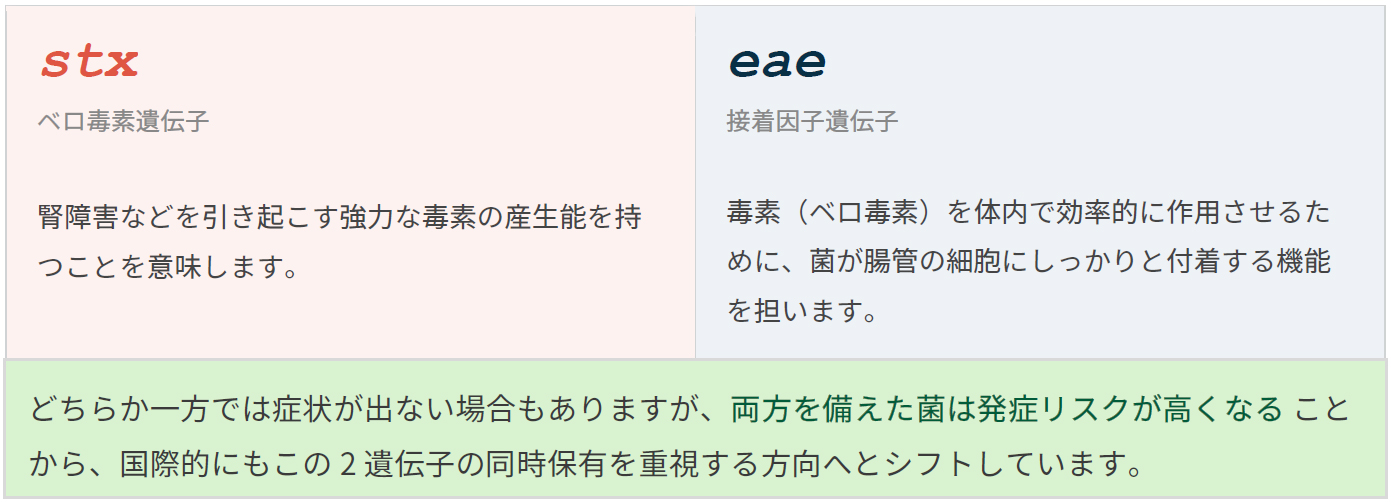
微生物検査の進化:従来法とstx/eaeスクリーニング法の違い
今回の通知改正は、こうした国際的な動向を反映し、stx/eae を検出するタイプのスクリーニング検査も正式な検査法の選択肢として認められるようになりました。
| 比較項目 | 従来の検査法(O抗原依存) | 新たな検査法(stx/eaeスクリーニング) |
|---|---|---|
| 検査の主眼 | 「菌の名前(血清型)」を特定する | 病原性関連遺伝子(stx/eae)を指標に評価する |
| 対象範囲 | 指定された特定のO抗原(O157, Top6等)のみ | 血清型に依存せず病原性関連遺伝子を検出可能 |
| 見逃しリスク | 指定外のO抗原を持つ病原菌を見逃す可能性あり | stx/eae遺伝子を標的とするため、見逃しを最小化 |
| 判定の速さ | 血清型別の特定に時間を要する場合がある | 最短15分〜60分で迅速にスクリーニング判定 |
| 国際適合性 | 国内基準が中心 | 米国(FSIS)や欧州など国際基準に準拠 |
| 推奨製品 | 病原菌検出アッセイ2 STEC 遺伝子スクリーニング(stx/eae)用 |
通知に定められた検査の流れ
農林水産省通知(別添1・別添3)では、スクリーニング検査と確認検査の2段階で STEC の検査を実施するよう定めています。
| 1 | 前増菌培養 BPW-ISO 等の培地を使用して、41.5 ℃ ± 1 ℃、10〜18 時間培養します。 |
|---|---|
| 2 | スクリーニング検査(遺伝子検出) 増菌培養液から DNA を抽出し、stx/eae遺伝子(およびO抗原遺伝子)を検出します。 ✓ ネオジェンジャパンの病原菌検出アッセイ2(stx/eae)はここで使用 |
| 3 | 結果の判定 stx/eae遺伝子の検出結果に基づき、陽性と判定された場合には確認検査へ進みます(判定条件は使用する検査法により異なります)。 |
| 4 | 確認検査(分離培養・血清型別・生化学試験) 免疫磁気ビーズ法による濃縮・分離培養を行い、血清型別試験・生化学的性状試験・stx/eae 確認試験を実施して最終判定します。 |
※ 検査の流れの詳細は農林水産省通知(別添1)および各スクリーニング法の仕様書をご参照ください。
病原菌検出アッセイ2 STEC 遺伝子スクリーニング(stx/eae)用 製品の特長
通知に例示された「病原菌検出アッセイ2 STEC 遺伝子スクリーニング(stx/eae)用」は、国際的な認証(Microval, AOAC PTM)を取得しており、迅速かつ正確なリスク管理をサポートします。
- 病原性を正確に特定:stx/eaeの両遺伝子を同時に検出。特定のO抗原に依存せず、真にリスクのある菌を見逃しません。
- 圧倒的な迅速性:最短15分で推定陽性判定、26時間で定性判定が可能。意思決定を加速させます。

- ◆ 病原性を正確に捉える
stx 及び eae の両遺伝子を同時に検出。感染リスクのある菌を見逃しません。
- ◆ 迅速な判定
装置での測定スタートから 60 分で陰性判定。最短 15 分で陽性判定が可能です。
- ◆ シンプルな操作
ピペットでの分注 2 回のみ。あとは装置が自動で測定します。
- ◆ 再増菌の手間なしで確認試験に直結
BPW-ISO 培地で前増菌するため、stx/eae 陽性時もそのまま確認試験に使用可能。さらに同一試料からサルモネラ属菌など他菌種の検査にも対応できます。
- ◆ 使いやすさも配慮
日本語対応ソフトウェア搭載で、初めてでも安心して導入いただけます。
今後の展望
今回の通知は輸出を前提としたものですが、検査の考え方自体が大きく転換されたことが重要です。今後、国内の検査においても O抗原だけでなく stx/eae で病原性を捉える視点が求められることが考えられます。
ネオジェンジャパンでは、国際的なリスク管理基準に対応した製品・サポートを通じて、お客様の検査体制強化を支援してまいります。
![[NEOGEN] ネオジェンジャパン](/assets/img/common/logo-neogen.png)